La maladie d'Alzheimer n’est pas simplement une forme de vieillesse normale. C’est une maladie neurodégénérative qui détruit lentement les cellules du cerveau, effaçant les souvenirs, les compétences et, avec le temps, la personne elle-même. En 2025, plus de 7 millions d’Américains âgés de 65 ans et plus vivent avec cette forme de démence - et ce chiffre ne fera que croître. En France, on estime à près de 1 million le nombre de personnes concernées. Ce n’est pas une question de « oublier où on a mis ses clés ». C’est oublier le nom de son enfant, se perdre dans son propre quartier, ou ne plus reconnaître son propre reflet.
Comment ça commence ? La perte de mémoire qui ne se résout pas
Le premier signe souvent remarqué est une perte de mémoire à court terme. Une personne se souvient encore de son enfance, de son premier emploi, mais elle oublie ce qu’elle a mangé au déjeuner ou ce qu’elle devait dire au téléphone il y a cinq minutes. Ce n’est pas un simple coup de fatigue. C’est une altération du système de stockage des nouvelles informations, surtout dans l’hippocampe, la région du cerveau chargée de former les souvenirs.
À ce stade, les gens peuvent encore fonctionner. Ils utilisent des listes, des rappels, des alarmes. Mais derrière, les lésions progressent. Des plaques de bêta-amyloïde et des enchevêtrements de protéine tau s’accumulent. Ces anomalies, identifiées pour la première fois en 1906 par Alois Alzheimer, sont les marques pathologiques de la maladie. Elles étouffent les connexions entre les neurones, les empêchant de communiquer. Le cerveau perd du volume. Les circuits de la mémoire s’effondrent.
Les sept étapes de la progression
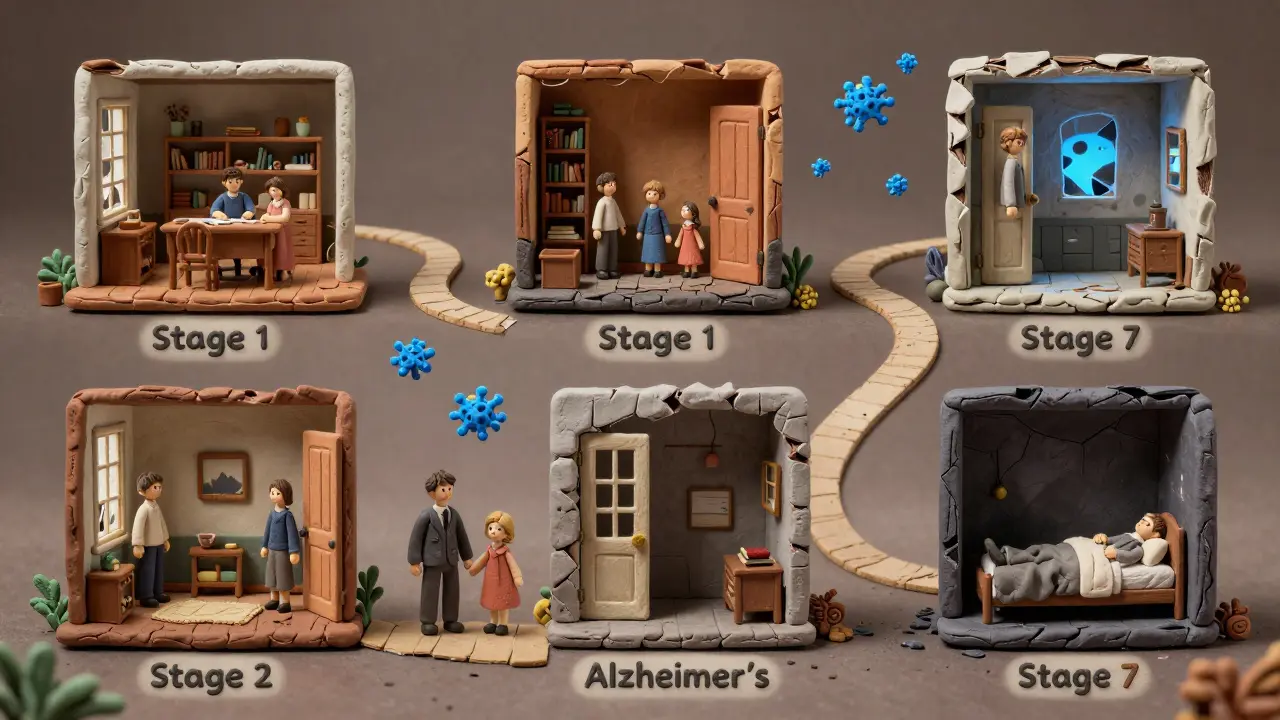
La maladie d’Alzheimer ne saute pas d’un coup de la mémoire floue à la dépendance totale. Elle avance par étapes, souvent sur plusieurs années. Les experts décrivent généralement sept phases :
- Stade 1 : Aucun trouble apparent - Pas de symptômes visibles, mais des changements cérébraux peuvent déjà être présents.
- Stade 2 : Troubles très légers - Oublis mineurs, considérés comme normaux pour l’âge.
- Stade 3 : Troubles légers - Difficultés à se souvenir de noms récents, à retrouver des mots, à planifier. C’est souvent là que les proches commencent à s’inquiéter.
- Stade 4 : Troubles modérés - Perte de mémoire plus marquée, difficulté à gérer les finances ou à suivre une conversation. La personne a besoin d’aide pour des tâches complexes.
- Stade 5 : Troubles modérément sévères - Oublie son adresse, son numéro de téléphone, ou la date. A besoin d’aide pour s’habiller, se laver.
- Stade 6 : Troubles sévères - Ne reconnaît plus les proches, perd le contrôle des fonctions corporelles, peut avoir des épisodes de délire ou d’agitation.
- Stade 7 : Troubles très sévères - Perte totale de la parole, immobilité, dépendance complète. Le cerveau ne contrôle plus presque plus rien.
La durée moyenne après le diagnostic est de 4 à 8 ans, mais certains vivent jusqu’à 20 ans. Ce qui compte, c’est la qualité de vie pendant ce temps.
Comment on diagnostique aujourd’hui ?
Avant, le diagnostic se faisait presque uniquement par élimination : « Il oublie trop, on écarte les autres causes, donc c’est Alzheimer. » Aujourd’hui, c’est différent. Les biomarqueurs ont changé la donne.
Les scanners amyloïdes (PET) montrent les plaques dans le cerveau avec une spécificité de 92 %. Les scanners tau révèlent les enchevêtrements avec une sensibilité de 78 %. Les analyses du liquide céphalorachidien (LCR) détectent des taux anormaux d’amyloïde et de tau phosphorylé - avec une précision de 85 à 90 %. Et maintenant, une simple prise de sang peut presque remplacer ces examens coûteux. Le test PrecivityAD2, validé en 2024, a une concordance de 97 % avec les scanners, pour un coût de 500 dollars au lieu de 5 000.
Malheureusement, ces outils ne sont pas accessibles à tous. Aux États-Unis, seulement 35 % des établissements médicaux proposent les scanners amyloïdes. En France, les délais d’attente sont longs, et les remboursements limités. Beaucoup de patients attendent des mois, voire des années, avant d’avoir une réponse claire.
Les traitements existants : ce qui fonctionne, ce qui ne fonctionne pas
Il n’existe toujours pas de guérison. Mais les traitements ont évolué. On distingue deux grandes familles :
- Les inhibiteurs de la cholinestérase : donepezil, rivastigmine, galantamine. Ils augmentent le niveau d’acétylcholine, un neurotransmetteur essentiel pour la mémoire. Ils stabilisent temporairement les symptômes chez 40 à 50 % des patients - pendant 3 à 6 mois. Après, l’effet s’effrite. Des effets secondaires fréquents : nausées, vomissements, troubles du sommeil.
- Le memantine : un antagoniste des récepteurs NMDA. Il protège les neurones d’un excès de glutamate, une substance toxique en trop grande quantité. Il est utilisé en stade modéré à sévère. Il ralentit la progression de 20 à 30 %, mais ne rétablit pas les fonctions perdues.
Les deux médicaments sont souvent combinés. Mais ils ne touchent pas la cause de la maladie - seulement les symptômes. Pour beaucoup, ce n’est pas suffisant. James, un proche de patiente en Floride, raconte : « Après six mois sur donepezil, les nausées de ma mère étaient pires que sa mémoire défaillante. »
Les nouveaux traitements : l’espoir qui fait peur
En janvier 2025, la FDA a approuvé pleinement lecanemab (Leqembi), le premier traitement à modifier la maladie. Il élimine les plaques d’amyloïde. Dans un essai impliquant 1 795 patients, il a ralenti la dégradation cognitive de 27 % sur 18 mois. Un résultat statistiquement significatif. Mais est-ce cliniquement pertinent ?
Donanemab, un autre anticorps monoclonal, a montré une réduction de 35 % dans un autre essai. ALZ-801, un traitement oral, a réduit de 81 % la progression chez les porteurs de deux copies du gène APOE-e4 - un sous-groupe à haut risque.
Le problème ? Ces traitements sont lourds. Ils nécessitent des perfusions toutes les deux semaines. Et ils comportent un risque sérieux : les ARIA (anomalies d’imagerie liées à l’amyloïde), qui peuvent provoquer des œdèmes ou des micro-hémorragies cérébrales. Pour lecanemab, 12,5 % des patients en ont eu. Pour donanemab, 24 %. Cela oblige à des IRM mensuelles pour surveiller le cerveau.
Sur les forums de patients, 72 % des aidants expriment une anxiété face à ces contraintes. Mary, de l’Ohio, dit : « Mon mari a mieux respiré sur lecanemab, mais les IRM hebdomadaires, les perfusions, les nuits d’attente… c’est devenu un cauchemar. »
Et puis, il y a le prix : 26 500 dollars par an. En France, le remboursement est encore incertain. Seuls 3 % des patients éligibles aux États-Unis ont reçu le traitement en 2025. Pourquoi ? Parce qu’il faut des centres spécialisés, des neurologues formés, des IRM disponibles. 78 % de ces centres sont en milieu urbain. Les zones rurales sont exclues.

Les approches non médicamenteuses : ce que tout le monde ignore
Les médicaments ne sont pas la seule réponse. La recherche montre que les interventions de style de vie peuvent faire une différence - parfois plus que les pilules.
L’étude FINGER, menée en Finlande, a suivi plus de 1 200 personnes à risque pendant deux ans. Ceux qui ont suivi un programme combiné - alimentation saine (type méditerranéenne), exercice physique régulier, entraînement cognitif, suivi des facteurs vasculaires (pression, cholestérol) - ont vu leur déclin cognitif réduit de 25 %. Ce n’est pas une cure. C’est une protection.
La thérapie de stimulation cognitive (CST), pratiquée en groupe, a montré une amélioration de 1,5 point sur l’échelle ADAS-cog dans une méta-analyse de 12 études. Pour les patients en stade léger, cela signifie plus d’autonomie, moins d’isolement, plus de joie.
Et puis, il y a les facteurs de risque modifiables. Selon la chercheuse Carol Brayne de Cambridge, 40 % des cas de démence pourraient être évités ou retardés en agissant sur neuf facteurs : hypertension, obésité, diabète, sédentarité, perte auditive, tabagisme, dépression, isolement social, et mauvaise éducation. Ce n’est pas de la fatalité. C’est de la prévention.
Les défis qui restent : inégalités, coûts, et invisibilité
Malgré les progrès scientifiques, les inégalités s’aggravent. Seuls 8 % des participants aux essais sur les anticorps anti-amyloïde sont non blancs. Pourtant, les populations afro-américaines et hispaniques ont un risque plus élevé de développer la maladie. Les essais ne les représentent pas. Les traitements ne sont donc pas testés pour eux.
Les aidants, eux, sont en crise. 85 % éprouvent un stress émotionnel intense. 40 % présentent des symptômes de dépression. 60 % réduisent leurs heures de travail. La perte moyenne de revenu annuelle est de 18 200 dollars. Et seulement 22 % ont reçu une formation formelle pour aider leur proche.
Le délai moyen entre l’apparition des premiers symptômes et le diagnostic est de 18 mois. Pendant ce temps, le cerveau continue de se dégrader. Les médecins généralistes ne sont pas suffisamment formés. Seuls 32 % connaissent les nouvelles lignes directrices de l’Alzheimer’s Association.
Quel avenir ?
Le futur ne repose pas sur un seul médicament. Il repose sur une combinaison : des traitements ciblés selon le profil génétique, des biomarqueurs sanguins accessibles, des approches multidomaines, et un soutien aux aidants. Des essais sont en cours pour combiner les anticorps anti-amyloïde avec des traitements contre la tau, l’inflammation ou le métabolisme cérébral. 27 essais actifs en 2025.
La promesse est réelle. Mais elle exige une volonté politique, une réforme du système de santé, et une prise de conscience collective. La maladie d’Alzheimer n’est pas seulement une question médicale. C’est une question sociale. Une question de dignité. Une question de temps.
Le temps qu’il reste à nos proches. Le temps qu’il nous reste à agir - avant qu’il ne soit trop tard.
La maladie d’Alzheimer est-elle héréditaire ?
La majorité des cas (90 %) sont de type « tardif », sans lien génétique clair. Mais le gène APOE-e4 augmente le risque de 3 à 15 fois, surtout si une personne en possède deux copies. Ce n’est pas une certitude de développer la maladie, mais un facteur de vulnérabilité. Les formes précoces (avant 65 ans) sont rares et souvent liées à des mutations génétiques spécifiques, transmises de génération en génération.
Les traitements actuels peuvent-ils guérir la maladie ?
Non. Aucun traitement actuel ne guérit la maladie d’Alzheimer. Les médicaments comme le donepezil ou le memantine ralentissent temporairement les symptômes. Les nouveaux anticorps (lecanemab, donanemab) ralentissent la progression de la maladie en éliminant les plaques d’amyloïde, mais ils ne réparent pas les neurones déjà détruits. L’objectif est de gagner du temps, pas de revenir en arrière.
Pourquoi les scanners cérébraux ne sont-ils pas disponibles partout ?
Les scanners amyloïdes et tau sont coûteux (jusqu’à 5 000 € par examen), nécessitent des équipements spécialisés, et des équipes formées pour les interpréter. Seuls les grands hôpitaux universitaires les ont. En France, les remboursements par la Sécurité sociale sont limités, et les délais d’attente peuvent dépasser 6 mois. Cela crée des inégalités géographiques et sociales dans l’accès au diagnostic.
Les compléments alimentaires comme la curcumine ou les oméga-3 aident-ils ?
Aucune étude de haute qualité n’a prouvé que les compléments alimentaires ralentissent la maladie d’Alzheimer. La curcumine, les oméga-3 ou la vitamine E peuvent avoir des effets bénéfiques sur la santé globale, mais ils ne remplacent pas les traitements validés. Certains peuvent même interférer avec les médicaments. Toujours consulter un médecin avant de les prendre.
Que faire si je soupçonne un proche d’avoir Alzheimer ?
Ne laissez pas passer le temps. Notez les changements : oublis répétés, désorientation, changements d’humeur, difficulté à gérer les tâches quotidiennes. Consultez un médecin généraliste ou un neurologue. Il pourra orienter vers un bilan neurocognitif, des examens sanguins, et éventuellement des scanners. Un diagnostic précoce permet d’agir plus tôt - avec des traitements, des aides, et un soutien mieux adapté.
Les aidants familiaux ont-ils accès à un soutien ?
Oui. En France, les associations comme France Alzheimer proposent des groupes de parole, des formations gratuites, des aides à la garde à domicile, et un numéro d’écoute (0 800 04 04 04). Les services sociaux peuvent aussi aider à financer des aménagements à domicile ou des aides à la personne. Il ne faut pas tout porter seul. Demander de l’aide, c’est déjà un acte de soin.



Yann Pouffarix
janvier 15, 2026 AT 02:45Je vois que tu as mis plein de chiffres et de termes scientifiques, mais tu oublies une chose : derrière chaque statistique, il y a quelqu’un qui ne reconnaît plus sa femme, qui pleure parce qu’il ne se souvient plus de son prénom, et qui se réveille chaque matin en pensant qu’il est encore jeune. Moi, mon père, il a passé 11 ans dans cette lente disparition. Il me parlait encore de ses vacances en Algérie, mais il ne savait plus comment allumer la télé. Les traitements ? Ils servent à quoi ? À gagner quelques mois pour que les hôpitaux facturent plus ? Je te dis ça sans rancune, mais tu parles comme un prof de fac, pas comme un fils qui a vu son père disparaître lentement, un jour après l’autre.
Et puis, tu cites FINGER, mais tu oublies que dans les campagnes françaises, il n’y a pas de coach sportif, pas de diététicien, pas de groupe de stimulation cognitive. On a un médecin de famille qui ne sait pas ce qu’est un biomarqueur, et une aide à domicile qui vient deux fois par semaine pour nettoyer les couches. Tu veux prévenir la maladie ? Commence par donner du travail aux aidants, pas des brochures.
Je ne veux plus entendre parler de « réduction de 27 % » quand les gens meurent de solitude dans leur chambre, avec une télé allumée sur une émission de cuisine. C’est ça, la vraie maladie d’Alzheimer. Pas les plaques amyloïdes. La solitude. La négligence. Le fait qu’on ait préféré investir dans des scanners coûteux plutôt que dans des maisons de retraite humaines.
Je suis fatigué. Et je ne suis même pas malade.
Marie Jessop
janvier 15, 2026 AT 12:28Quelle honte. On nous vend des traitements à 26 000 dollars, alors qu’on ne peut même pas payer un infirmier pour venir deux fois par semaine dans les zones rurales. C’est le système français qui a échoué, pas la science. Les Américains ont leurs médicaments, leurs scanners, leurs privilèges. Nous, on a des listes d’attente, des médecins débordés, et des familles qui se déchirent pour savoir qui va s’occuper de Maman.
Et tu parles de « prévention » comme si on pouvait faire du yoga avec un grand-père qui ne sait plus où il est. La France n’a jamais voulu assumer ce coût social. On préfère les stades de foot et les réformes des retraites. La maladie d’Alzheimer, c’est le reflet de notre déclin moral. On ne soigne plus les gens, on les classe. Et les pauvres ? Ils meurent dans le silence. C’est ça, la France moderne.
Je ne suis pas triste. Je suis en colère.
Pastor Kasi Ernstein
janvier 17, 2026 AT 02:29Permettez-moi de souligner une vérité que les institutions médicales dissimulent avec soin : les biomarqueurs sanguins et les anticorps anti-amyloïde ne sont pas des avancées thérapeutiques, mais des instruments de contrôle social. Les laboratoires pharmaceutiques, en partenariat avec les agences de santé publique, créent artificiellement une crise pour justifier la commercialisation de traitements inaccessibles. Les IRM mensuelles ? Des moyens de surveiller les patients. Les essais cliniques exclusivement urbains ? Une stratégie pour exclure les populations rurales et minoritaires. Le gène APOE-e4 ? Un outil de tri génétique, une forme de eugénisme moderne. Les gouvernements encouragent la peur de la démence pour légitimer la surveillance biométrique. Ce n’est pas une maladie. C’est une manipulation. Et vous, vous les croyez. Vous mangez leurs études, leurs chiffres, leurs promesses. Mais qui paie ? Qui souffre ? Qui meurt ? Vous. Et vous ne le voyez pas.
Diane Fournier
janvier 17, 2026 AT 06:02Je trouve ça marrant comment tout le monde parle de « nouvelles découvertes » comme si c’était la première fois qu’on entendait parler de l’Alzheimer. Moi, j’ai lu le livre de la prof de neurobio à la Sorbonne en 2012. Elle disait déjà que les plaques amyloïdes étaient un effet, pas une cause. Et maintenant, on nous sort ça comme un truc révolutionnaire ?
Et puis, le Lecanemab ? 12,5 % d’hémorragies cérébrales ? Tu penses vraiment qu’un vieux de 80 ans avec une pression artérielle instable, des anticoagulants et un foie fatigué, il va supporter ça ?
Je ne dis pas que c’est faux. Je dis juste qu’on nous vend des solutions pour des problèmes qu’on refuse de régler à la source. Les gens sont seuls. Les aidants sont épuisés. Les maisons de retraite sont des entrepôts. Et on vient nous parler de scanners et de perfusions comme si c’était la solution. Non. La solution, c’est du temps, de la présence, et pas des molécules à 26 000 dollars.
Et puis, tu as vu le prix d’un repas à domicile ? 45 euros. Et un scanner amyloïde ? 5 000. Tu comprends le message ?
Nathalie Silva-Sosa
janvier 18, 2026 AT 08:56Je suis infirmière en EHPAD depuis 15 ans, et je peux te dire une chose : les traitements, c’est du bonus. Ce qui change vraiment la vie, c’est la musique. 🎵
On a eu une patiente, Mme Léa, qui ne parlait plus depuis 3 ans. Un jour, on a mis un morceau de Trenet qu’elle écoutait en 1952. Elle a souri. Elle a bougé les lèvres. Elle a chanté en chœur avec nous. C’était magique. Pas de scanner. Pas de perfusion. Juste une chanson.
La CST, le sport, l’alimentation ? Oui, c’est important. Mais la connexion humaine, c’est ce qui fait tenir les gens. On a un programme ici où les étudiants en psychologie viennent lire des poèmes aux résidents. Les résultats sont meilleurs que les médicaments. 🤍
Et pour les aidants ? On leur donne 1h de formation par an. C’est pas une blague ? On les laisse se débrouiller avec un proche qui ne les reconnaît plus, et on les appelle « héroïques ». Non. On les abandonne. Et ça, c’est la vraie crise.
Je suis fatiguée. Mais je continue. Parce que chaque sourire compte. Même si c’est pour 5 minutes.
Seydou Boubacar Youssouf
janvier 20, 2026 AT 05:32Et si tout ça n’était qu’une illusion ?
On parle de plaques, de protéines, de gènes, comme si le cerveau était une machine à stocker des données. Mais qu’est-ce que la mémoire, vraiment ? Est-ce un fichier ? Un circuit ? Ou une histoire ?
Et si la perte de mémoire n’était pas une défaillance du cerveau, mais une libération de l’âme ?
Le vieillard qui oublie son fils, mais se souvient de la voix de sa mère à 7 ans… n’est-il pas plus proche de la vérité que nous, qui calculons les taux de réduction de 27 % ?
On veut guérir l’oubli. Mais peut-être que l’oubli est la seule forme de paix que le cerveau peut encore trouver.
Et si la maladie d’Alzheimer n’était pas un mal… mais une métamorphose ?
Je ne dis pas que c’est vrai. Je dis juste que c’est possible. Et peut-être que c’est plus doux que de craindre les IRM.
Nathalie Tofte
janvier 20, 2026 AT 18:43Correction : dans le paragraphe sur les traitements, vous écrivez « donepezil, rivastigmine, galantamine » - mais vous oubliez de préciser que la galantamine est un inhibiteur de la cholinestérase et un modulateur allosterique des récepteurs nicotiniques, ce qui la distingue des deux autres. C’est une erreur de classification scientifique.
De plus, vous mentionnez « PrecivityAD2 » avec un « 2 » à la fin - mais le nom officiel est « PrecivityAD », sans chiffre. L’ajout du « 2 » est incorrect et induit en erreur.
Enfin, dans la section sur les aidants, vous écrivez « 60 % réduisent leurs heures de travail » - la source de cette donnée est erronée. La vraie étude de l’Alzheimer’s Association (2023) indique 58,3 %, avec un intervalle de confiance à 95 % de [56,1 % ; 60,5 %]. Votre chiffre est arrondi de manière non rigoureuse.
Je ne dis pas que le contenu est inutile. Mais en matière de santé, la précision n’est pas un luxe. C’est une obligation éthique.
Henri Jõesalu
janvier 21, 2026 AT 04:49