Tag: FDA
Pourquoi les médicaments génériques ont une apparence différente : le rôle des lois sur les marques
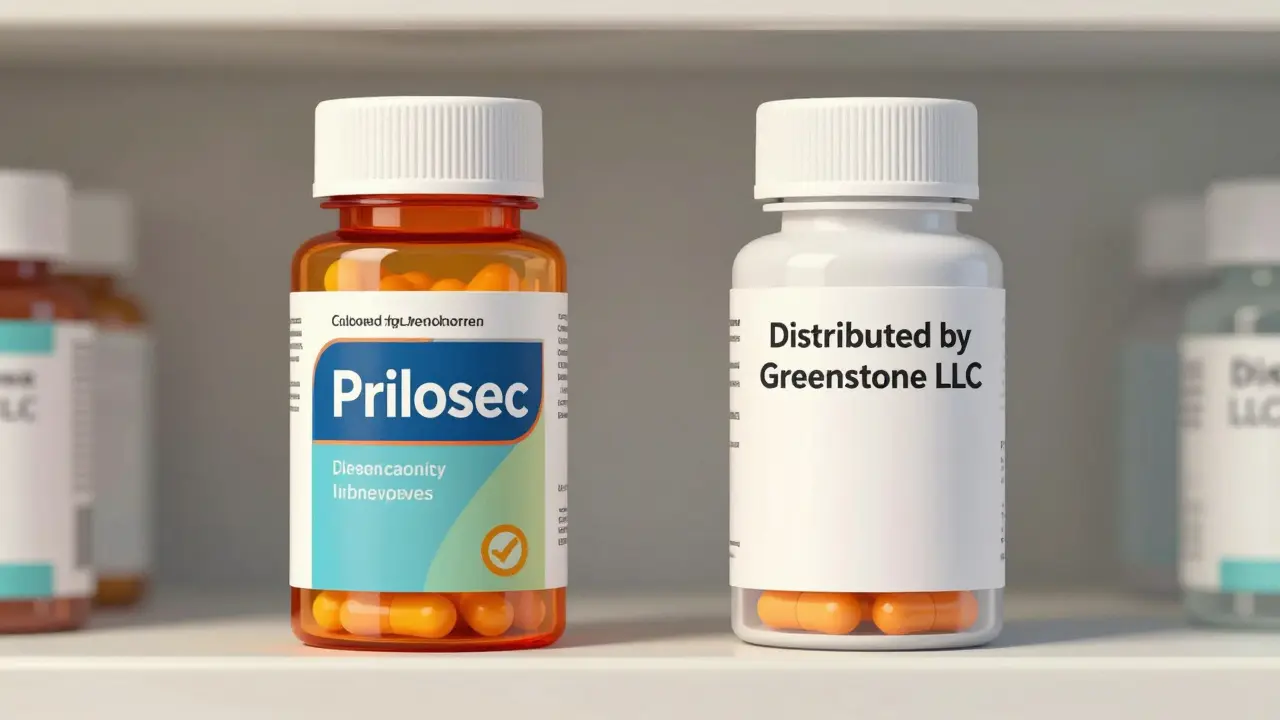
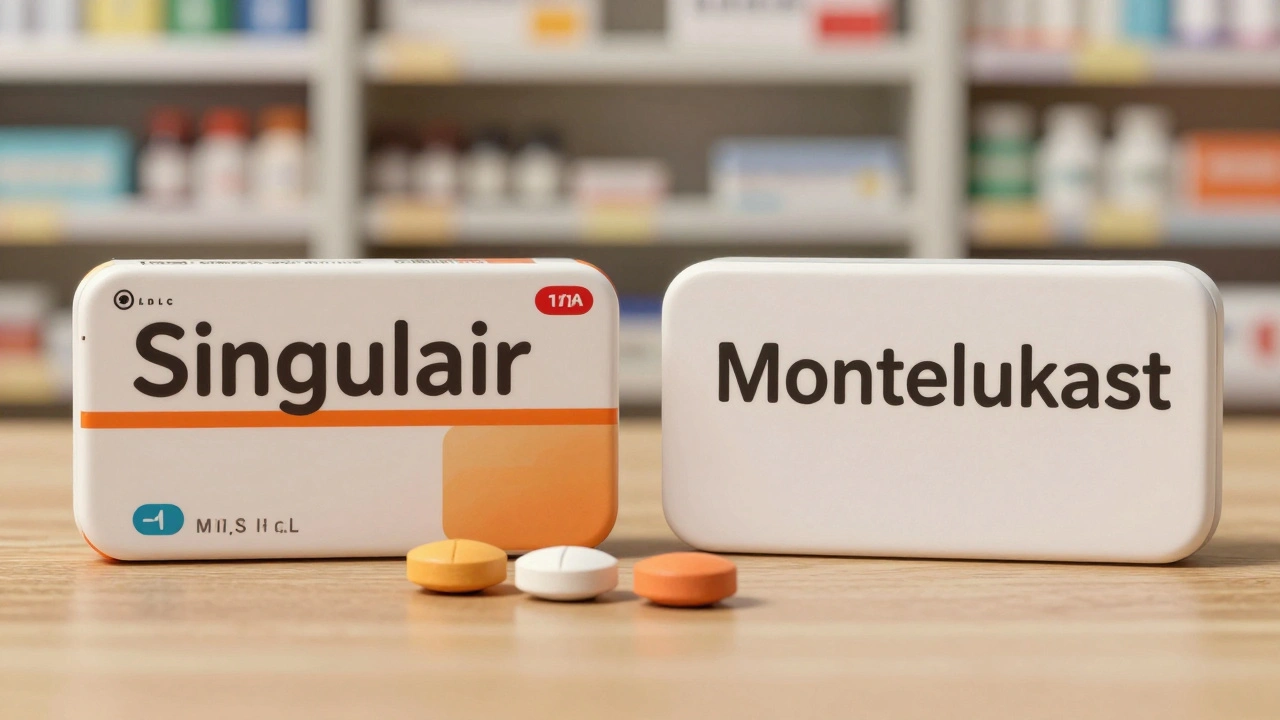
Les médicaments génériques ont une apparence différente des médicaments de marque à cause des lois sur les marques commerciales. Cette différence, qui concerne la couleur, la forme ou la taille, n'affecte en rien leur efficacité. Ils contiennent la même substance active et agissent de la même manière.
Continuer la lectureFormulations à libération modifiée : les spécificités de l'équivalence bioéquivalente
Les formulations à libération modifiée exigent des méthodes d'évaluation de l'équivalence bioéquivalente bien plus complexes que les comprimés classiques. Découvrez les exigences réglementaires de la FDA et de l'EMA, les pièges techniques, et pourquoi ces génériques coûtent jusqu'à 7 millions de dollars de plus.
Continuer la lectureEmballage et étiquetage : comment identifier les génériques autorisés
Apprenez à identifier les génériques autorisés grâce à leur emballage et étiquetage. Découvrez comment lire le code NDC, distinguer les vrais génériques des versions de marque, et choisir le médicament le plus sûr et le plus économique.
Continuer la lectureHatch-Waxman Act : la fondation de la politique américaine des médicaments génériques
La loi Hatch-Waxman de 1984 a révolutionné l'accès aux médicaments génériques aux États-Unis en équilibrant innovation et concurrence. Elle a permis des économies de plus de 300 milliards de dollars par an, mais aussi des abus par les laboratoires pharmaceutiques.
Continuer la lectureFDA Drug Shortage Database : comment vérifier la disponibilité des médicaments
Découvrez comment utiliser la base de données officielle de la FDA pour vérifier les pénuries de médicaments aux États-Unis. Informations précises, méthodes de recherche, limites et conseils pratiques pour patients et professionnels.
Continuer la lectureMédicaments génériques : définition complète et caractéristiques essentielles
Les médicaments génériques sont identiques aux marques en efficacité et sécurité, mais jusqu'à 85 % moins chers. Découvrez comment ils sont testés, approuvés et pourquoi ils sont la meilleure option pour la plupart des traitements.
Continuer la lectureLes préférences des patients : les génériques autorisés sont-ils choisis en pratique ?
Les génériques autorisés sont identiques aux médicaments de marque, mais vendus sans nom de marque. Les patients les préfèrent souvent pour leur similarité, mais le prix les pousse vers les génériques classiques après quelques mois.
Continuer la lectureUnités d'assurance qualité : une supervision indépendante pour garantir la production
Les unités d'assurance qualité doivent être indépendantes pour garantir la sécurité des produits pharmaceutiques. Découvrez pourquoi cette séparation est obligatoire, comment l'organiser, et les risques de la négliger.
Continuer la lecturePublicité trompeuse dans les génériques : risques juridiques et règles à respecter
La publicité trompeuse sur les médicaments génériques met en danger la santé des patients et viole la loi. Découvrez les règles de la FDA, les risques juridiques et comment reconnaître les mensonges dans les campagnes publicitaires.
Continuer la lectureGénériques autorisés vs génériques traditionnels : quelles différences réelles ?
Les génériques autorisés sont identiques aux médicaments de marque, tandis que les génériques traditionnels peuvent avoir des différences dans les ingrédients inactifs. Découvrez quand choisir l’un ou l’autre pour votre santé.
Continuer la lectureSections d'expérience post-commercialisation : ce que signifient réellement ces effets secondaires
Les sections d'expérience post-commercialisation révèlent les effets secondaires rares et graves détectés après la mise sur le marché des médicaments. Comprendre ces données est essentiel pour éviter les erreurs de prescription et protéger les patients.
Continuer la lectureHatch-Waxman Act : la loi fédérale qui révolutionne l'approbation des médicaments génériques aux États-Unis
La loi Hatch-Waxman de 1984 a révolutionné l'accès aux médicaments génériques aux États-Unis en créant un processus d'approbation rapide et économique, tout en protégeant l'innovation pharmaceutique. Elle a permis des économies de plus de 1,7 billion de dollars.
Continuer la lecture